ผู้แต่ง | Zhang Tailiu
บรรณาธิการ | Xi
มะเร็งปอดเป็นสาเหตุสำคัญของการเสียชีวิตจากโรคมะเร็งทั่วโลกในปัจจุบันผู้ป่วยที่เป็นมะเร็งปอดชนิด non-small-cell ( NSCLC ) ที่ไม่สามารถแก้ไขได้ส่วนใหญ่ใช้การรักษาด้วยเคมีบำบัด ( CRT ) แต่อัตราการรอดชีวิตระยะยาวอยู่ในระดับต่ำ ผู้ป่วยส่วนใหญ่มีประสบการณ์การดำเนินโรค การศึกษาล่าสุดแสดง CRT หลังจากใช้การรักษาด้วยการควบรวมกิจการ – ภูมิคุ้มกันด่านปราบปราม (ภูมิคุ้มกันด่านยับยั้ง, ไอซีไอ ) ในผู้ป่วย NSCLC ขั้นสูงสามารถปรับปรุงปราศจากโรคและการรอดชีวิตโดยรวม[1] อย่างไรก็ตามผู้ป่วยบางรายสามารถรักษาให้หายขาดได้ด้วยการรักษาด้วย CRT เท่านั้นและผู้ป่วยส่วนใหญ่มีการกำเริบของเนื้องอกแม้จะมีการรักษาแบบรวม ICI [2]ซึ่งบ่งชี้ว่าผู้ป่วยต้องได้รับการวิเคราะห์เพื่อกำหนดทางเลือกการรักษาส่วนบุคคล
เนื้องอกปล่อย ctDNA (การไหลเวียนของ DNA เนื้องอก) สู่เลือดรอบนอกและสามารถตรวจจับและวัดปริมาณในการตรวจชิ้นเนื้อของเหลวเพื่อตรวจสอบการตอบสนองการรักษา หลังการรักษา MRD ctDNA (โรคที่เหลือโมเลกุล s, MRD ) สามารถทำนายความก้าวหน้าของหลายประเภทของการเกิดซ้ำของเนื้องอกและ[3] จากการศึกษาแสดงให้เห็นว่าการตรวจ MRD หลังการรักษาด้วย CRT นั้นมีความไวสูงและสามารถทำนายการพัฒนาของโรค NSCLC แบบก้าวหน้าได้ อย่างไรก็ตามยังไม่ชัดเจนว่าการใช้การรวม ICI ในผู้ป่วย NSCLC สามารถปรับปรุงการพยากรณ์โรคทางคลินิกได้หรือไม่
2020 วันที่ 20 มกราคมมหาวิทยาลัย Stanford ของสหรัฐอเมริกาแอชเอ Alizadeh, Maximilian Diehnและศูนย์มะเร็ง MD Anderson สตีเว่นเอชหลินทีมในมะเร็งธรรมชาติตีพิมพ์รายงานสิทธิในการไหลเวียนของการเปลี่ยนแปลงดีเอ็นเอเนื้องอกทำนายได้รับประโยชน์จากการควบรวมกิจการ ภูมิคุ้มกันในขั้นสูงในประเทศ บทความเกี่ยวกับมะเร็งปอดที่ไม่ใช่เซลล์ขนาดเล็กเปิดเผยว่าการทดสอบ ctDNA สามารถช่วยทำนายผลประโยชน์ทางคลินิกของผู้ป่วย NSCLC หลังจากได้รับการรักษาด้วยการรวม ICI

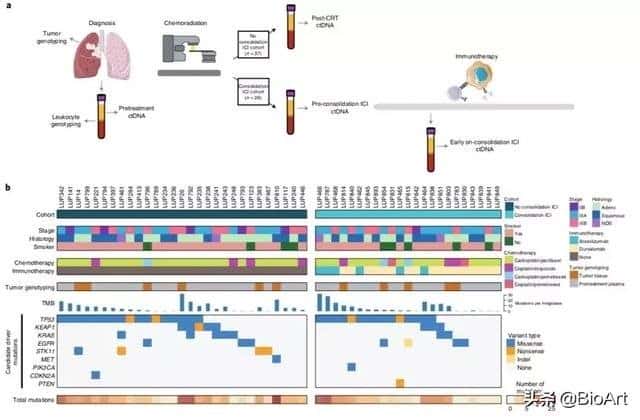
นักวิจัยได้ทำการเก็บตัวอย่างเลือดและเนื้อเยื่อ 218 ครั้งจากผู้ป่วย 65 รายที่มี NSCLC ขั้นสูงในพื้นที่ซึ่งได้รับ CRT (n = 37) หรือ CRT + ICI Consolidation therapy (n = 28) การวิเคราะห์ ctDNA ก่อนการรักษาด้วย CRT นั้น ctDNA ถูกตรวจพบใน 78% ของผู้ป่วยในกลุ่มการรักษา CRT และ 75% ในกลุ่มการรักษา CRT + ICI การรวมกันไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างทั้งสอง การวิเคราะห์กลุ่มการรักษา CRT พบว่าผู้ป่วยที่ไม่ได้ตรวจพบ ctDNA หลังการรักษาด้วย CRT (100%) เป็นอิสระจากความก้าวหน้า ( FFP ) ภายใน 24 เดือนในขณะที่ผู้ป่วยที่ตรวจพบ ctDNA ภายใน 24 เดือน ทั้งสองมีอาการกำเริบ (0%) ซึ่งสอดคล้องกับการศึกษาก่อนหน้านี้และ MRD มีค่าทำนายสูงสำหรับความเสี่ยงของการเกิดโรคหลังจากการรักษา CRT ctDNA ได้รับการตรวจสอบในระหว่างการรักษาด้วย ICI ในกลุ่มการรักษาแบบรวม CRT + ICI พบว่าผู้ป่วย 8 รายที่เสื่อมสภาพจากโรคหลังจากการรักษาด้วย ICI สามารถตรวจพบ ctDNA (100%) ก่อนและระหว่างการดำเนินโรคและตรวจพบอัตราส่วน ctDNA วิทยาศาสตร์แสดงให้เห็นว่าโรคนี้ก้าวหน้าไป 4.1 เดือนก่อนหน้านี้ การตรวจหา ctDNA ก่อนหรือในช่วงต้นของการรักษาด้วย ICI เป็นตัวทำนายที่มีประสิทธิภาพของความเสี่ยงของการเกิดโรคการก้าวหน้าของโรคที่เกิดขึ้นใน 6 (86%) ของผู้ป่วย 7 คนที่ตรวจพบ ctDNA ในช่วงแรกของการรักษา ICI เทียบกับผู้ป่วยเพียง 15 คน ความก้าวหน้าของโรคเกิดขึ้นใน 3 (13%) การตรวจหา ctDNA ในระหว่างการรักษาด้วย ICI เป็นเครื่องมือพยากรณ์โรคที่มีประสิทธิภาพ
ามารถทำการทดสอบ ctDNA หลังจากการรักษาด้วย CRT เพื่อระบุผู้รับผลประโยชน์ของการรักษาด้วยการรวม ICI ได้หรือไม่? ผู้ป่วยส่วนใหญ่ในกลุ่มรักษาแบบรวม CRT + ICI (n = 13, 59%) ไม่ได้ตรวจพบ ctDNA หลังจากได้รับการรักษาด้วย CRT และการพยากรณ์โรคของพวกเขาดี 80% ของผู้ป่วยนั้นไม่มีความก้าวหน้าของโรคภายใน 1 ปี ตัวอย่างเช่นผู้ป่วย LUP838 (คล้ายกับผู้ป่วยส่วนใหญ่) มีมะเร็งเซลล์ squamous ระยะ IIIA ในปอดและตรวจพบ ctDNA ก่อนการรักษาด้วย CRT แต่ไม่มีการตรวจพบ ctDNA 1.5 เดือนหลังจากสิ้นสุดการรักษาด้วย CRT และก่อนการรักษาด้วย ICI จาก 1.5 เดือนหลังจากการรักษาด้วย ICI จนถึง 15 เดือนการติดตามไม่สามารถตรวจพบ ctDNA และไม่มีอาการของโรค ในทางตรงกันข้ามอย่างนี้ผู้ป่วย LUP893 ที่มี IIIB ปอดเซลล์มะเร็ง squamous และการรักษา CRT ส่งผลให้ตรวจพบ ctDNA ไม่นานหลังจากเริ่มการรักษาแบบรวมศูนย์ (ICI) ผู้ป่วยก็เริ่มมีอาการไอและหายใจสั้นลงแม้จะมีการรักษาอย่างแข็งขันเขาก็เสียชีวิตด้วยการหายใจล้มเหลว การชันสูตรพลิกศพแสดงให้เห็นถึงความรุนแรงในระดับทวิภาคีเฉียบพลันและปอดบวมเนื้อเยื่อนอกบริเวณการรักษาด้วยรังสีหรือเกิดจากภูมิคุ้มกันบำบัดและผู้ป่วยไม่แสดงอาการของโรคมะเร็งที่เหลือ สถานะการพยากรณ์โรคของ ctDNA ที่ได้รับหรือไม่ได้รับการรักษารวม ICI หลังการรักษา CRT ถูกเปรียบเทียบและไม่พบความแตกต่างทางสถิติระหว่างทั้งสองกลุ่มในแง่ของความก้าวหน้าของโรคที่ปราศจากโรคนั่นคือผู้ป่วยที่ไม่มีการตรวจจับ ctDNA .
ในทางตรงกันข้ามผู้ป่วยที่ตรวจพบ ctDNA หลังการรักษาด้วย CRT ได้รับการรักษาด้วย ICI และ FFP ของพวกเขาดีกว่าผู้ป่วยที่ตรวจพบ ctDNA หลังการรักษาด้วย CRT อย่างมีนัยสำคัญ แต่ไม่ได้รับการรักษาด้วยการรวม ICI จลนศาสตร์ของ ctDNA ระหว่างการบำบัดแบบรวมศูนย์ของ ICI สามารถระบุผู้ป่วยที่ได้รับประโยชน์จาก ICI ได้หรือไม่? ความเข้มข้นของ ctDNA ในเลือดถูกวัดก่อนและในช่วงต้นของการรักษาด้วย ICI และพบสองโหมดตอบสนองต่อ ctDNA: 1) ความเข้มข้นของ ctDNA เพิ่มขึ้นในช่วงแรกของการรักษาด้วย ICI (50%) 2) ความเข้มข้น ctDNA ลดลงในช่วงแรก การเพิ่มความเข้มข้นของ ctDNA ในระหว่างการรักษาด้วย ICI หมายถึงการพยากรณ์โรคที่ไม่ดีผู้ป่วยทั้งหมดที่มี ctDNA ที่เพิ่มขึ้นจะมีความก้าวหน้าของโรคภายใน 4.5 เดือนหลังจากเริ่มการรักษาด้วย ICI และขาดการตอบสนองต่อภูมิคุ้มกัน นอกจากนี้การพยากรณ์โรคของผู้ป่วยที่มีความเข้มข้นของ ctDNA สูงในระหว่างการรักษาด้วย ICI ไม่แตกต่างจากผู้ป่วยที่ตรวจพบ ctDNA หลังการรักษาด้วย CRT แต่ไม่ได้รับการรักษาแบบรวม ICI นั่นคือความเข้มข้นของ ctDNA ที่เพิ่มขึ้นในช่วงต้นของการรักษาด้วย ICI สามารถใช้ระบุผู้ป่วยที่ดื้อต่อภูมิคุ้มกัน อย่างไรก็ตามผู้ป่วยที่ลด ctDNA ในช่วงต้นของการรักษาด้วย ICI มีการพยากรณ์โรคที่ดีโดยมี FFP 1 ปีถึง 100% และระยะเวลาการดำเนินโรคที่ปลอดโรคของพวกเขานานกว่าผู้ป่วย ctDNA ที่ตรวจพบหลังจาก CRT แต่ไม่ได้รับการรักษาด้วย ICI ในทางตรงกันข้าม 94% ของผู้ป่วยที่ตรวจพบ ctDNA หลังการรักษาด้วย CRT แต่ไม่ได้รับ ICI พัฒนาความก้าวหน้าของโรคในระยะไกล นั่นคือการตรวจสอบ ctDNA หลังการรักษาด้วย CRT และการรักษาแบบบูรณาการในช่วงต้นของ ICI สามารถระบุผู้ป่วยที่ได้รับประโยชน์มากที่สุดจากการรักษาแบบรวม ICI
โดยสรุปการวิจัยแสดงให้เห็นว่าผู้ป่วยที่มี MRD ที่ได้รับ MRT หลังจากมะเร็งปอดที่ไม่ใช่เซลล์ขนาดเล็กได้รับการรักษาแบบบูรณาการ ICI สามารถปรับปรุงการพยากรณ์โรคของพวกเขาและการตรวจสอบ ctDNA สามารถช่วยรวบรวมยาเฉพาะบุคคลสำหรับการรักษา .
ลิงค์เดิม:
ผู้ผลิต: Xiao Xianzi
อ้างอิง
- Antonia, SJ etal. การอยู่รอดโดยรวมกับ durvalumab หลังการรักษาด้วยเคมีบำบัดในระยะ IIINSCLC N. Engl. J. Med. 379, 2342–2350 (2018)
แบรดลีย์ 2. ผล JD et al, ระยะยาวของ RTOG 0617: … 3 เฟสสุ่มเปรียบเทียบมาตรฐานเมื่อเทียบกับปริมาณที่สูงปริมาณ conformalchemoradiation ± cetuximab บำบัดสำหรับขั้นตอนที่สามของ NSCLC … Int เจสรวง Radiat.Oncol.Biol 99, S105 (2017)
- Abbosh, C. et al. การวิเคราะห์ ctDNA Phylogenetic แสดงให้เห็นวิวัฒนาการของมะเร็งปอดระยะที่แทบจะไม่ธรรมชาติ 545, 446 – 451 (2017)






